La vacuna de Pfizer es 100% eficaz en adolescentes de 12 a 15 años: ¿Cuándo será aprobada?
Share this article
Subscribe
By pressing the Subscribe button, you confirm that you have read our Privacy Policy.
Últimas noticias


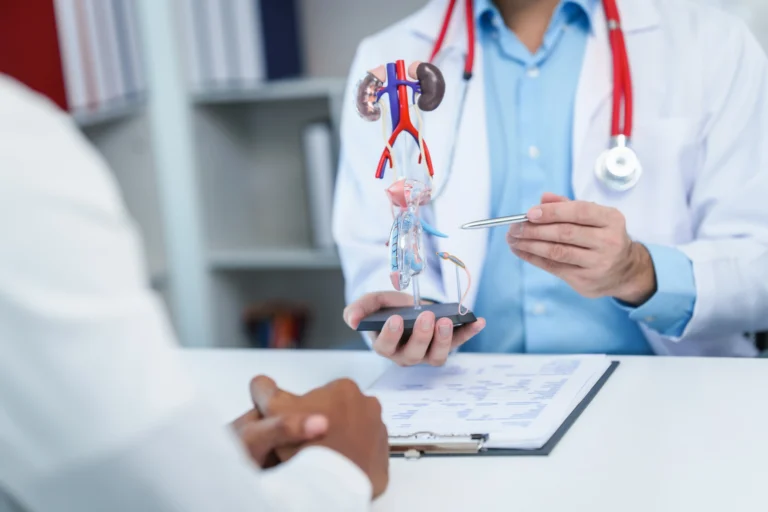

Lámparas UV: ¿Puede la manicure producir cáncer de piel?
26 noviembre, 2025

Dolor por escoliosis: ¿qué hacer para sentirme mejor?
19 noviembre, 2025

¿Qué significa que un país tenga alta vigilancia sanitaria?
7 noviembre, 2025
Featured Categories
Más Noticias


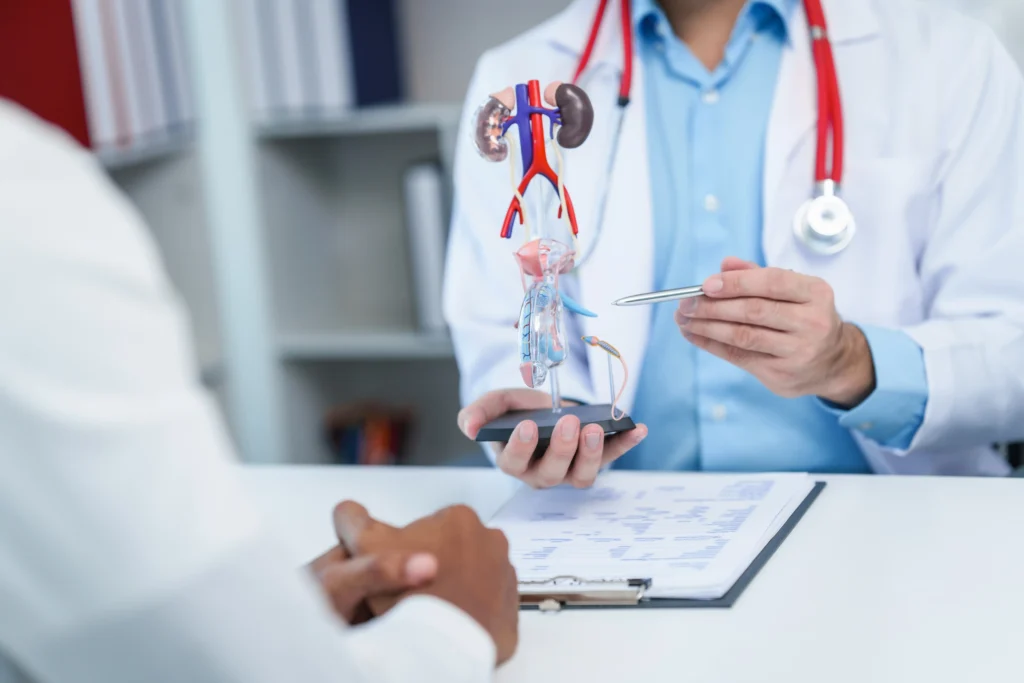

Lámparas UV: ¿Puede la manicure producir cáncer de piel?
26 noviembre, 2025

Dolor por escoliosis: ¿qué hacer para sentirme mejor?
19 noviembre, 2025

¿Qué significa que un país tenga alta vigilancia sanitaria?
7 noviembre, 2025
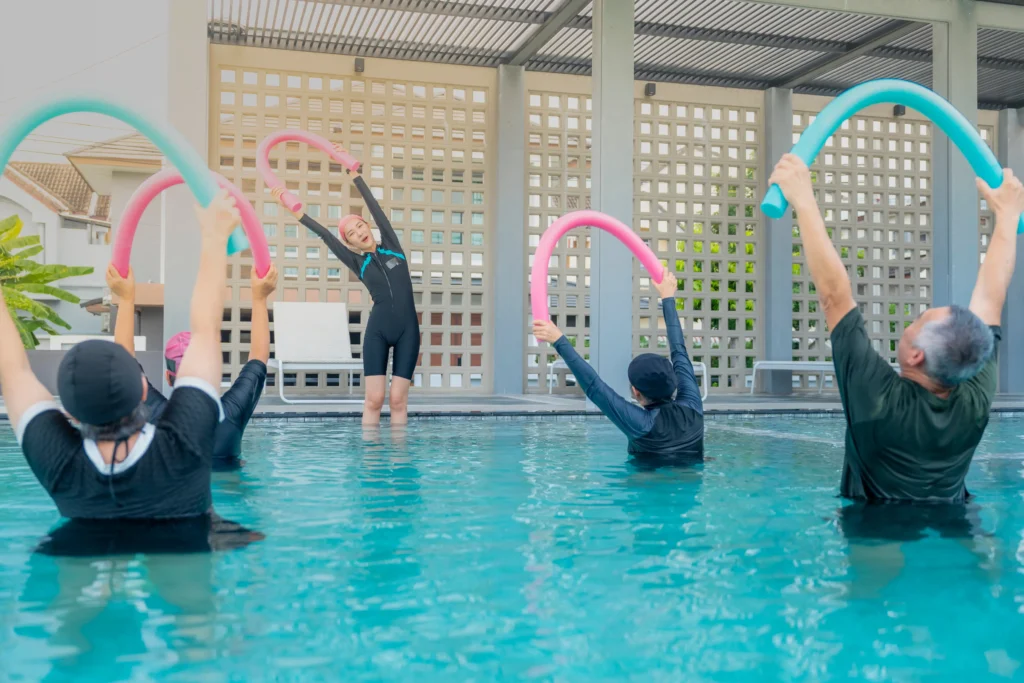
¿Por qué el ejercicio acuático es tan beneficioso para la salud?
6 noviembre, 2025

¿Qué alimentos les hacen más daño a nuestros riñones?
23 octubre, 2025
